潘越、周一鸣团队开发锰-聚多巴胺纳米免疫调节剂,通过CD44介导的双靶向递送机制,重塑肾癌免疫微环境
论文题目:潘越、周一鸣团队开发锰-聚多巴胺纳米免疫调节剂,通过CD44介导的双靶向递送机制,重塑肾癌免疫微环境。
通讯作者:潘越;周一鸣
第一作者:杜玉菲;麦译尹
论文发表刊物:Advanced healthcare materials
|
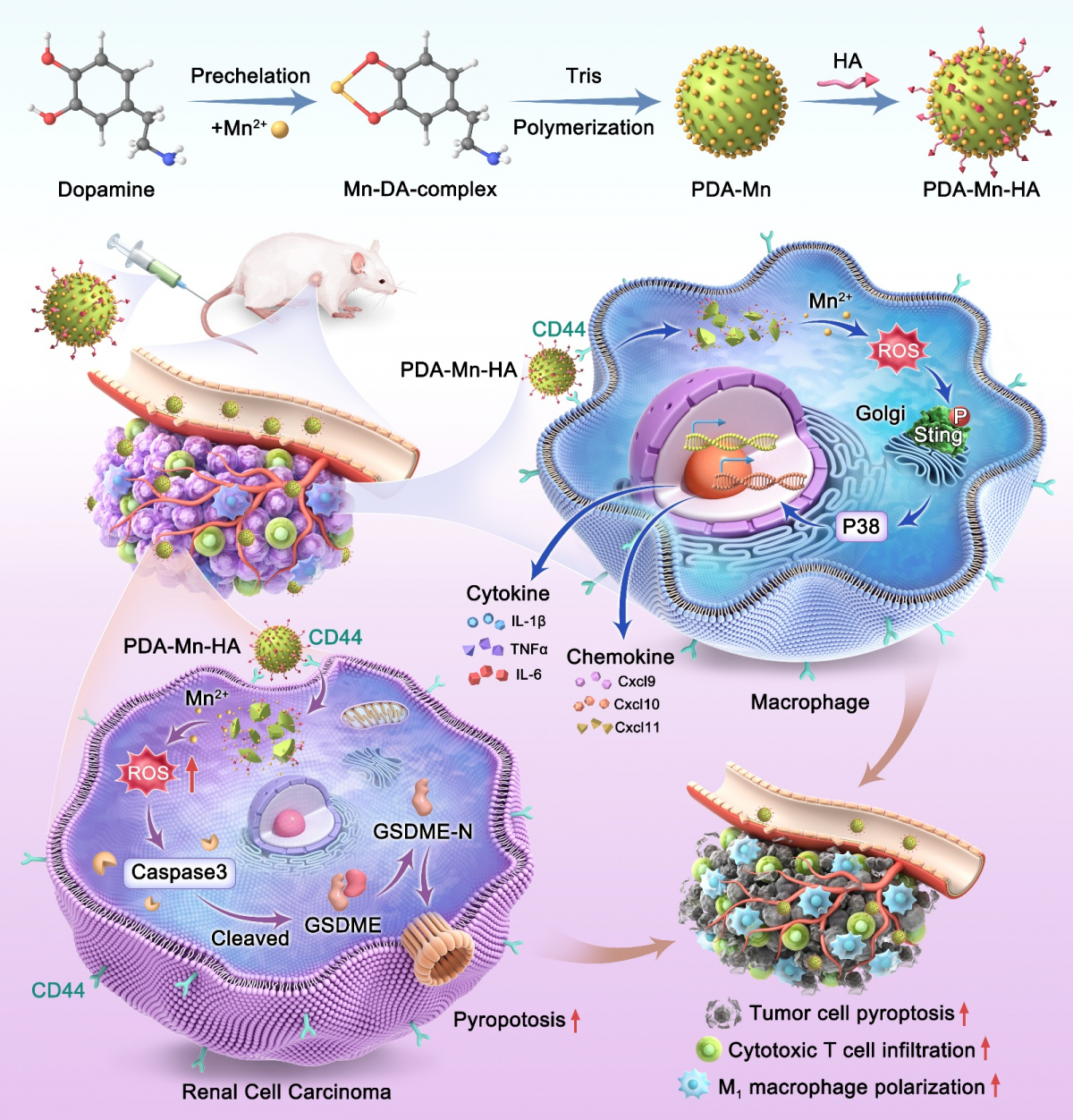
图1. PDA-Mn-HA 作为多功能纳米免疫调节剂在肾细胞癌中的应用示意图。 |
【研究背景】
肾癌是泌尿系统最常见的恶性肿瘤之一,其中主要是肾细胞癌(RCC)。肾细胞癌发病隐匿且对放化疗耐受,免疫治疗是晚期患者的主要治疗手段,但免疫治疗耐药显著限制了疗效提升。肿瘤相关巨噬细胞(TAMs)促进免疫逃逸和耐药,但肾癌中TAMs的靶向调控机制尚未明确。开发兼具靶向性和免疫微环境重塑功能的新型纳米制剂,是突破当前治疗瓶颈的重要方向。
【主要发现】
本研究构建了透明质酸修饰的锰-聚多巴胺纳米免疫调节剂(PDA-Mn-HA),可靶向CD44受体,在酸性肿瘤微环境中释放Mn²⁺。其通过激活ROS-STING-MAPK通路诱导TAMs向M1型极化,并通过ROS-caspase-3/GSDME轴触发肿瘤细胞焦亡,显著抑制肾癌进展且具有良好的安全性。
【研究意义】
该研究构建的针对肾癌及TAMs的纳米免疫调节剂,解决了锰制剂靶向性差和神经毒性的难题,为肾癌治疗提供了新策略。其多重功能设计为调控肾癌免疫微环境开辟了新路径,具有重要临床转化价值。
【课题组介绍】
潘越:中山大学孙逸仙纪念医院研究员,博导,广东省杰出青年基金获得者、中山大学“百人计划”引进中青年杰出人才、孙逸仙纪念医院“高层次人才特别支持计划”青年拔尖人才。美国Brandeis University博士毕业,哈佛医学院博士后。研究领域为材料生物医学,如肿瘤的多模态影像诊断和放射协同治疗等。申请人以通讯(含共同)作者身份发表论文50余篇。论文总引用5600余次,H指数42,单篇引用超过100次以上的论文15篇(google scholar)。荣获英国皇家化学会“Top 1%高被引中国作者”。获授权专利5项(申请人均排名第一),部分成果已进入转化阶段。多次在国际国内学术会议上进行大会邀请报告。主持国自然面上、广东省杰青、广州市重点研发计划(医疗卫生与健康关键技术)等基金项目,作为核心成员参与国家和广东省重点研发计划。入选高层次创新创业引才“境外世界名校博士计划”,“高层次人才特别支持计划”三个三青年拔尖人才项目;荣获英国皇家化学会“Top 1%高被引中国作者”,“Journal of Materials Chemistry B新锐科学家”,“华夏医学科技奖三等奖”等。研究成果被国自然基金委网站, Faculty of 1000, Advanced Science News和Chemistry World等以专题文章报道和推荐。担任国际组织工程与再生医学学会亚太年会的分会主席、国际材料研究会亚洲大会的组织委员会委员、广东省精准医学应用学会分子影像分会常务委员和医工结合分会常务委员。担任多种国际高水平期刊的客座主编和特邀审稿人。
课题组网站:https://lab.rjmart.cn/#/10035/PanLab
周一鸣:中山大学孙逸仙纪念医院研究员,博导,海外高层次人才引进青年项目,广东省珠江人才青年拔尖项目,中山大学百人计划入选者。周一鸣研究员在日本综合研究大学院大学(SOKENDAI)和国立生理学研究所获得博士学位,之后在哈佛大学医学院 附属BWH 医院和 Broad 研究所进行了博士后研究,2018 年12月加入中山大学孙逸仙纪念医院。周一鸣研究员主要聚焦在肾脏疾病和自身免疫性疾病的发病机制及相关靶点和药物的研发。利用单细胞组学、干细胞、类器官等技术,研究肾脏疾病和自免病的发病机制,同时研发药物用于相关疾病的治疗。至今在国际SCI期刊发表学术论文共计30余篇,其中以第一作者和通讯作者在Science、Nature Communications、EBioMedicine、Advanced Science、Cell Reports、Advanced healthcare materials和Biomaterials等多个国际知名刊物发表文章,文章累计被引用次数超过2500多次。曾获得日本生理学会青年学者奖,BWH医院心肾杰出研究奖等。曾主持国自然青年项目、面上项目及日本学术振兴会青年项目等。
论文链接:
https://pubmed.ncbi.nlm.nih.gov/40394938/
阅读二维码:
![]()







 粤公网安备 44010402003003号
粤公网安备 44010402003003号 