【临床研究设计部】研究者发起的临床研究合同签署指南
一、适用范围
本指南适用于研究者发起的临床研究与外单位合作签署合同,根据《中山大学孙逸仙纪念医院合同管理办法》制定。
二、合同签署流程
(一)合同拟定要求
原则上合同要求使用我院模板拟定,并只能以修订模式编辑“非限制编辑区域”。若必须使用外单位合同模板或修改“限制编辑区域”,应满足《合同自查表》(附件7或附件8)的要求,且由于需经医院律师审核,会大大增加审核时间,请项目负责人慎重考虑。
(二)合同拟定规范
合同的内容包括(但不限于)协议条款、保密责任、文章发表及知识产权、项目实施要求、项目预计实施时间、入组例数、物资供应、保险、与研究相关损害的赔偿、经费预算及支付方式等。
我院合同模板包括《合作协议》(外单位作为发起者时适用)(附件1)、《科研合作协议》(我院作为发起者时适用)(附件2)、《逸仙临床研究培育项目/5010多中心合作协议》(附件3)、《CRC服务协议》(附件4)、《补充协议》(附件5)、《技术服务合同》(附件6)。
(三)合同的形式审核流程
因涉及赔偿、经费条款的审核,故需待临床研究方案及知情同意书定稿后才能进行合同形式审核流程。
1.使用我院合同模板,仅编辑“非限制编辑区域”的合同
1.1形式审查
①项目负责人将确认后的电子版合同、我院在有效期内的伦理批件、合同他方法人证书/营业执照、法人签字授权函(如适用)、委托代理人身份证明(如适用)、获得伦理批准的知情同意书,邮件命名为“合同审查-合同类型-项目负责人-项目简称”,发至临床研究设计部(以下简称“设计部”)邮箱。
②设计部以批注的形式提出意见。约5-10个工作日反馈意见,具体时间视资料完整程度而定。以上为一次审核所需时间,退回修改需重新走流程。
③项目负责人按意见修改,需以修订模式提交设计部。
2.未使用我院合同模板或修改“限制编辑区域”的合同
2.1项目负责人合同自查
项目负责人参照合同自查表(附件7或附件8)进行自查。
2.2形式审查
①在项目负责人完成合同自查后,将确认后的电子版合同、我院在有效期内的伦理批件、合同他方法人证书/营业执照、法人签字授权函(如适用)、委托代理人身份证明(如适用)、获得伦理批准的知情同意书、合同自查表扫描版,邮件命名为“合同审查-合同类型-项目负责人-项目简称”,发至设计部邮箱。
②设计部交医院法律顾问审核,约20-25个工作日提出设计部及律师审核意见,具体时间视资料完整程度及合同的复杂程度而定。以上为一次审核所需时间,退回修改需重新走流程。为节省时间,应严格按律师要求修改,勿反复退回修改。
③项目负责人按意见修改,需以修订模式提交设计部。
(四)合同的OA多部门会审流程
形式审查后,设计部通知项目负责人填写我院OA《合同审查表》,要求在OA上提交清洁版合同、我院有效的伦理批件、合同他方法人证书、法人签字授权函(如适用)、委托代理人身份证明(如适用)及其他要求的文件。设计部按医院要求提交有关业务部门、分管副院长审查。
(五)合同的签署流程
1.待OA会审流程通过后,项目负责人向设计部递交纸质版合同。原则上应先由对方单位法定代表人/代理人签署,加盖对方单位公章及骑缝章,经我院项目负责人签字。
2.设计部尽快递交院办,院办处理时间一般需要一周。
3.合同签署完成后,设计部通知项目负责人领取。
三、研究者发起的临床研究合同审核流程图
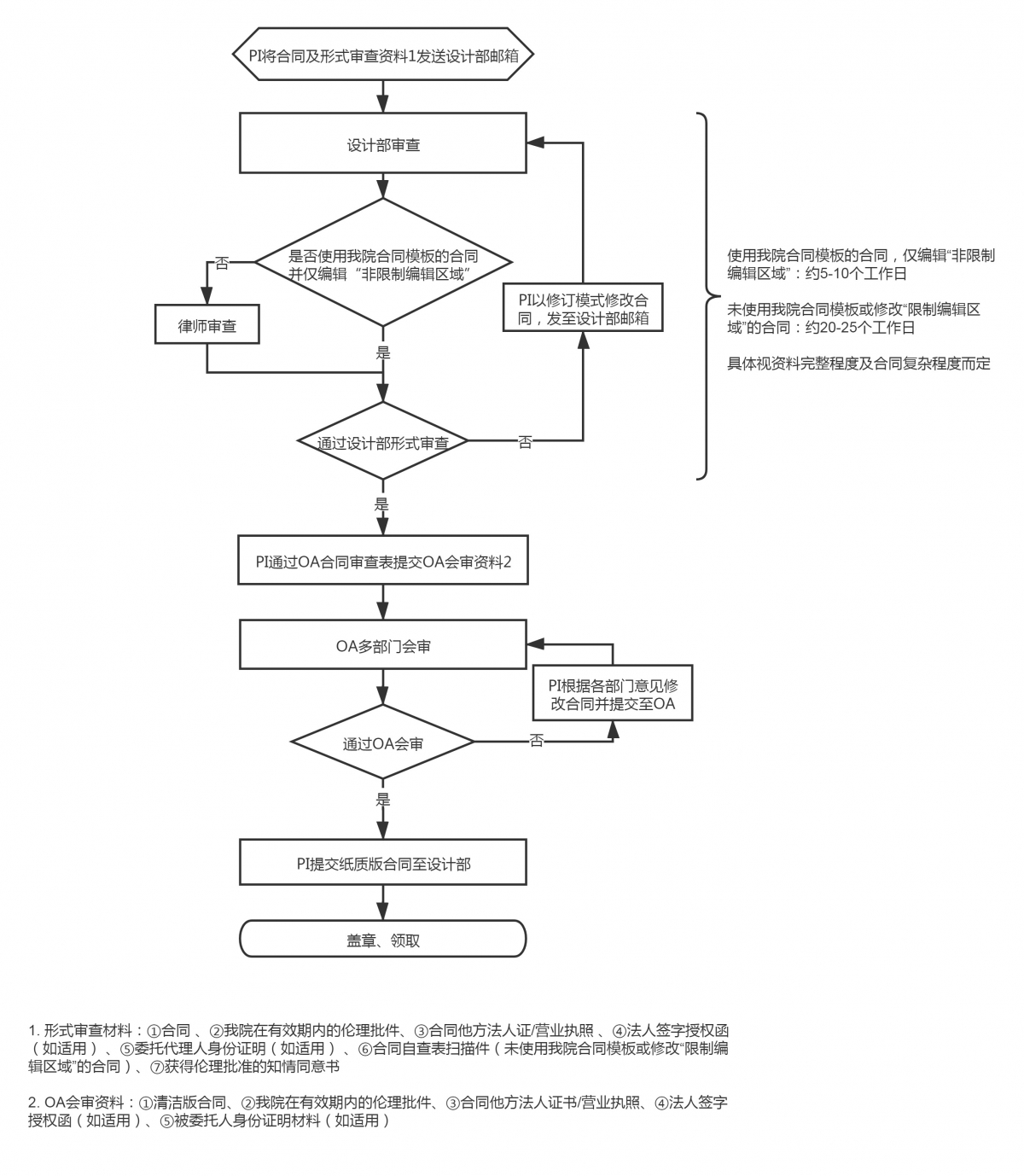
四、其他注意事项
指南中所涉及附件请参见我院OA文件,具体路径:OA首页(下拉)→单位文档→临床研究中心文档(全院可见)→【临床研究设计部】工作指南→研究者发起的临床研究合同签署指南。
如有问题,请联系临床研究设计部,地址:北院区岭南楼26楼,电话:020-81336505,邮箱:sys_iit@163.com。






 粤公网安备 44010402003003号
粤公网安备 44010402003003号 